Aktinium
89
Ac
Skupina
n/a
Perioda
7
Blok
f
Protony
Elektrony
Neutrony
89
89
138
Hlavní vlastnosti
Atomové číslo
89
Atomová hmotnost
[227]
Hmotnostní číslo
227
Kategorie
Aktinoidy
Barva
Stříbrná
Radioaktivní
Ano
Z řeckého aktis, aktinos, znamenající paprsek nebo svazek
Krystalografická soustava
Krychlová plošně centrovaná
Historie
André-Louis Debierne, a French chemist, discovered actinium in 1899.
He separated it from pitchblende residues left by Marie and Pierre Curie after they had extracted radium.
Friedrich Oskar Giesel independently discovered actinium in 1902 as a substance being similar to lanthanum.
He separated it from pitchblende residues left by Marie and Pierre Curie after they had extracted radium.
Friedrich Oskar Giesel independently discovered actinium in 1902 as a substance being similar to lanthanum.
Elektronů v obalu
2, 8, 18, 32, 18, 9, 2
Elektronová konfigurace
[Rn] 6d1 7s2
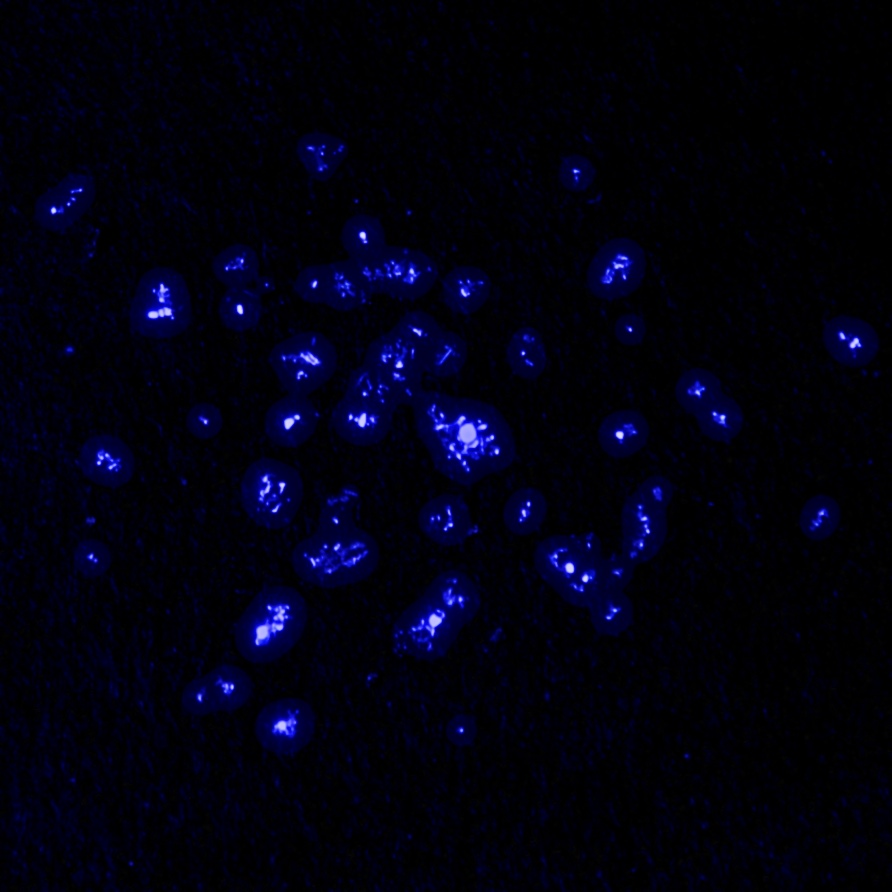
Actinium glows in the dark with a pale blue light
Fyzické vlastnosti
Skupenství
Pevná
Hustota
10,07 g/cm3
Teplota tání
1323,15 K | 1050 °C | 1922 °F
Teplota varu
3471,15 K | 3198 °C | 5788,4 °F
Skupenské teplo tání
14 kJ/mol
Skupenské teplo varu
400 kJ/mol
Měrná tepelná kapacita
0,12 J/g·K
Hojnost v zemské kůře
n/a
Hojnost ve vesmíru
n/a
Číslo CAS
7440-34-8
PubChem CID číslo
n/a
Atomové vlastnosti
Atomový poloměr
-
Kovalentní poloměr
215 pm
Elektronegativita
1,1 (Paulingova stupnice)
Ionizační potenciál
5,17 eV
Molární objem
22,54 cm3/mol
Tepelná vodivost
0,12 W/cm·K
Oxidační čísla
3
Aplikace
Actinium is used as an active element of radioisotope thermoelectric generators, for example in spacecraft.
The medium half-life of 227Ac makes it very convenient radioactive isotope in modeling the slow vertical mixing of oceanic waters.
225Ac is applied in medicine to produce 213Bi in a reusable generator or can be used alone as an agent for radiation therapy.
The medium half-life of 227Ac makes it very convenient radioactive isotope in modeling the slow vertical mixing of oceanic waters.
225Ac is applied in medicine to produce 213Bi in a reusable generator or can be used alone as an agent for radiation therapy.
Aktinium je vysoce radioaktivní
Izotopy
Stabilní izotopy
-Nestabilní izotopy
206Ac, 207Ac, 208Ac, 209Ac, 210Ac, 211Ac, 212Ac, 213Ac, 214Ac, 215Ac, 216Ac, 217Ac, 218Ac, 219Ac, 220Ac, 221Ac, 222Ac, 223Ac, 224Ac, 225Ac, 226Ac, 227Ac, 228Ac, 229Ac, 230Ac, 231Ac, 232Ac, 233Ac, 234Ac, 235Ac, 236Ac